Byron Druss
À la seconde où vous ouvrez de l'eau ultrapure, elle commence à se dégrader. En 48 heures, une eau qui commençait à 18 MΩ·cm (norme de type 1) peut chuter à environ 1 MΩ·cm. Cela représente une perte de pureté de 94 %.
La plupart des gens ne réalisent pas que cela se produit aussi rapidement. De nombreux laboratoires achètent de l’eau ultra pure en bouteille, l’utilisent pendant des jours ou des semaines, puis se demandent pourquoi leurs tests sont incohérents. La vérité : une fois que l'eau rencontre l'air, elle change.
L'eau ultra-pure a « faim ». Il capte le dioxyde de carbone de l’air dès qu’il est exposé. Ce CO₂ se transforme en acide carbonique, qui se décompose en ions. Les ions ruinent la résistivité.
Voici à quelle vitesse elle chute :
On dirait toujours de l'eau. Mais ce n'est plus ultra-pur.
Mauvaise eau = mauvaises données.
Dans tous les cas, vous menez une bataille perdue d'avance.
Ce n'est pas seulement un problème de pureté. C'est un problème d'efficacité.
Pourquoi Les systèmes d'eau de laboratoire ultrapure sont meilleurs
Un système au point d'utilisation produit de l'eau ultra pure lorsque vous en avez besoin. Pas de stockage. Aucune supposition. Aucune dégradation.
Avantages :
Pour la plupart laboratoires, le système s’amortit en 12 à 18 mois. Les laboratoires très occupés s'arrêtent souvent encore plus rapidement.
Comment savoir si l'eau ultrapure stockée est mauvaise ?
Vérifiez-la avec un résistimètre ou un conductimètre. En dessous de 10 MΩ·cm ? Trop compromis pour les travaux sensibles.
Quelles applications sont les plus sensibles ?
La HPLC et la spécification de masse sont les plus touchées. Mais la culture cellulaire et la biologie moléculaire en pâtissent également. Même une « simple » préparation de tampon peut mal tourner avec de l'eau dégradée.
Est-il difficile de passer à un système ?
Pas vraiment. L'installation prend généralement 1 à 2 jours. Une fois qu'il fonctionnera, vous vous demanderez pourquoi vous avez acheté des bouteilles.
Si je dois stocker de l'eau, quel est le meilleur ?
Utilisez de petits récipients scellés. Ne conservez pas plus de 48 heures s’il s’agit d’un travail critique. La couverture d'azote peut l'étirer, mais elle ajoute des tracas et des coûts.
Acheter de l'eau ultrapure en bouteille semble facile. Mais il ne reste pas pur une fois ouvert. Il se désintègre rapidement et entraîne des coûts cachés : données erronées, perte de temps et fuites budgétaires.
Un système d'eau de laboratoire ultra-pur résout tout cela. Vous obtenez de l’eau ultra pure à la demande, toujours fraîche, toujours prête. À long terme, c'est le choix le plus intelligent et le moins cher.
Et pour ceux qui s'intéressent à la science :
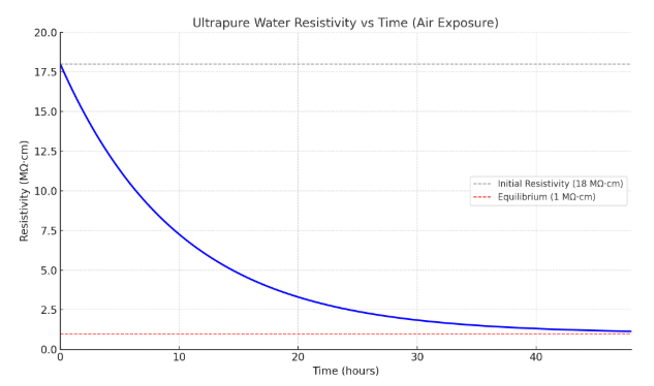
Le graphique illustre comment la résistivité de l'eau ultrapure chute de 18 MΩ·cm à environ 1 MΩ·cm en 48 heures lorsqu'elle s'équilibre avec l'air. Ce déclin est principalement dû à l'absorption du CO₂, qui forme de l'acide carbonique et libère des ions, réduisant ainsi la résistivité.
Le graphique est basé sur un modèle simulé, et non sur des données expérimentales directes. Voici le contexte :
Modèle de données utilisé
R(t)=17⋅e−kt+1R(t) = 17 \cdot e^{-kt} + 1
où :
Comprendre la dégradation de la qualité de l'eau aide les laboratoires à prendre des décisions éclairées concernant leur stratégie en matière d'eau ultra pure. La bonne approche dépend de vos applications spécifiques, des exigences de flux de travail et des normes de qualité.
