Byron Druss
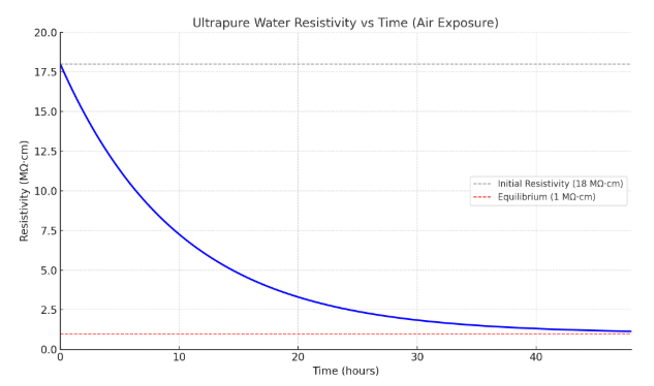
En el momento en que abres el agua ultrapura, comienza a ir cuesta abajo. En 48 horas, el agua que comenzó en 18 MΩ·cm (estándar Tipo 1) puede bajar a aproximadamente 1 MΩ·cm. Esto representa una pérdida de pureza del 94 %.
La mayoría de las personas no se dan cuenta de que sucede tan rápido. Muchos laboratorios compran agua ultrapura embotellada, la usan durante días o semanas y luego se preguntan por qué sus análisis son inconsistentes. La verdad: una vez que el agua se encuentra con el aire, cambia.
El agua ultrapura tiene “hambruna”. Capta el dióxido de carbono del aire en el momento en que queda expuesto. Ese CO₂ se convierte en ácido carbónico, que se descompone en iones. Los iones arruinan la resistividad.
Así de rápido cae:
Todavía parece agua. Pero ya no es ultrapuro.
Agua de mala calidad = datos incorrectos.
De cualquier manera, estás librando una batalla perdida.
No es solo un problema de pureza. Es un problema de eficiencia.
Por qué Los sistemas de agua de laboratorio ultrapura son mejores
Un sistema de punto de uso produce agua ultrapura cuando la necesita. Sin almacenamiento. Sin adivinanzas. Sin degradación.
Beneficios:
Para la mayoría de los laboratorios, el sistema se amortiza solo en 12 a 18 meses. Los laboratorios ocupados a menudo se recuperan aún más rápido.
¿Cómo puedo saber si el agua ultrapura almacenada se ha echado a perder?
Compruébelo con un medidor de resistividad o conductividad. ¿Por debajo de 10 MΩ·cm? Demasiado comprometido para trabajos sensibles.
¿Qué aplicaciones son las más sensibles?
HPLC y especificación de masas son las más afectadas. Pero el cultivo celular y la biología molecular también sufren un gran impacto. Incluso la preparación “simple” del buffer puede salir mal con agua degradada.
¿Es difícil cambiar a un sistema?
En realidad, no. La instalación suele tardar entre 1 y 2 días. Una vez que esté funcionando, te preguntarás por qué compraste botellas.
Si debo almacenar agua, ¿qué es mejor?
Usa recipientes pequeños sellados. No lo dejes más de 48 horas si es para trabajos críticos. La capa de nitrógeno puede estirarla, pero añade molestias y costos.
Comprar agua ultrapura embotellada es fácil. Pero no permanece puro una vez abierto. Se descompone rápidamente y causa costos ocultos: datos incorrectos, pérdida de tiempo y pérdidas de presupuesto.
Un sistema de agua de laboratorio ultrapura resuelve todo eso. Obtendrá agua ultrapura cuando la necesite, siempre fresca y siempre lista. A largo plazo, es la opción más inteligente y económica.
Y para aquellos interesados en la ciencia:
El gráfico ilustra cómo la resistividad del agua ultrapura cae de 18 MΩ·cm a alrededor de 1 MΩ·cm en 48 horas a medida que se equilibra con el aire. Esta disminución se debe principalmente a la absorción de CO₂, que forma ácido carbónico y libera iones, lo que reduce la resistividad.
El gráfico se basa en un modelo simulado, no en datos experimentales directos. Estos son los antecedentes:
Modelo de datos utilizado
R(t)=17⋅e−kt+1R(t) = 17 \cdot e^{-kt} + 1
donde:
Comprender la degradación de la calidad del agua ayuda a los laboratorios a tomar decisiones informadas sobre su estrategia de agua ultrapura. El enfoque correcto depende de sus aplicaciones específicas, requisitos de flujo de trabajo y estándares de calidad.
